政策法规||本周重磅政策法规概览(21.03.15-21.03.19)
NMPA/CDE/药典委公布药品/医疗器械相关内容本周集锦。
01
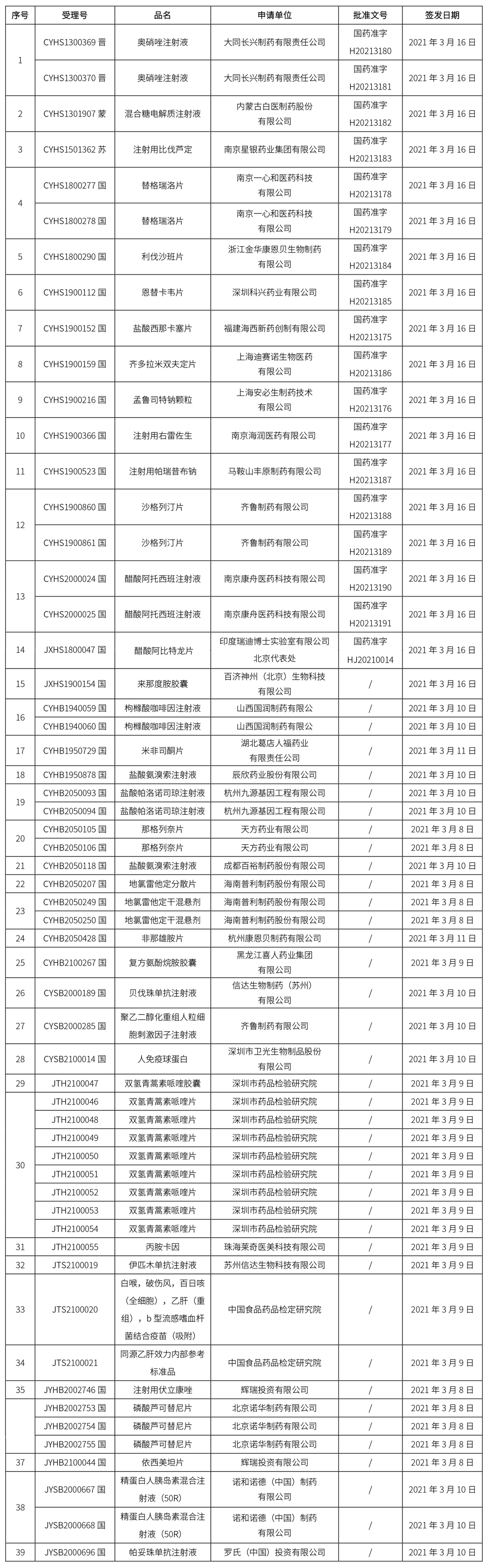
本周共发布39个品种批准证明文件待领取通知,其中一致性评价品种8个,注射剂品种16个。
关于发布《创新药(化学药)临床试验期间药学变更技术指导原则(试行)》的通告(2021年第22号)

扫描下方二维码
查看相关信息

关于硝酸咪康唑阴道片处方药转换为非处方药的公告(2021年第34号)

扫描下方二维码
查看相关信息

关于发布重组胶原蛋白生物材料命名指导原则的通告(2021年第21号)
扫描下方二维码
查看相关信息

05
关于发布医疗器械行业标准《口腔胶原膜通用技术要求》的公告(2021年第39号)
扫描下方二维码
查看相关信息

关于发布《皮肤外用化学仿制药研究技术指导原则(试行)》的通告(2021年第23号)

扫描下方二维码
查看相关信息

关于修订阿魏酸钠注射制剂说明书的公告(2021年第43号)
扫描下方二维码
查看相关信息

关于修订氟哌啶醇制剂说明书的公告(2021年 第40号)
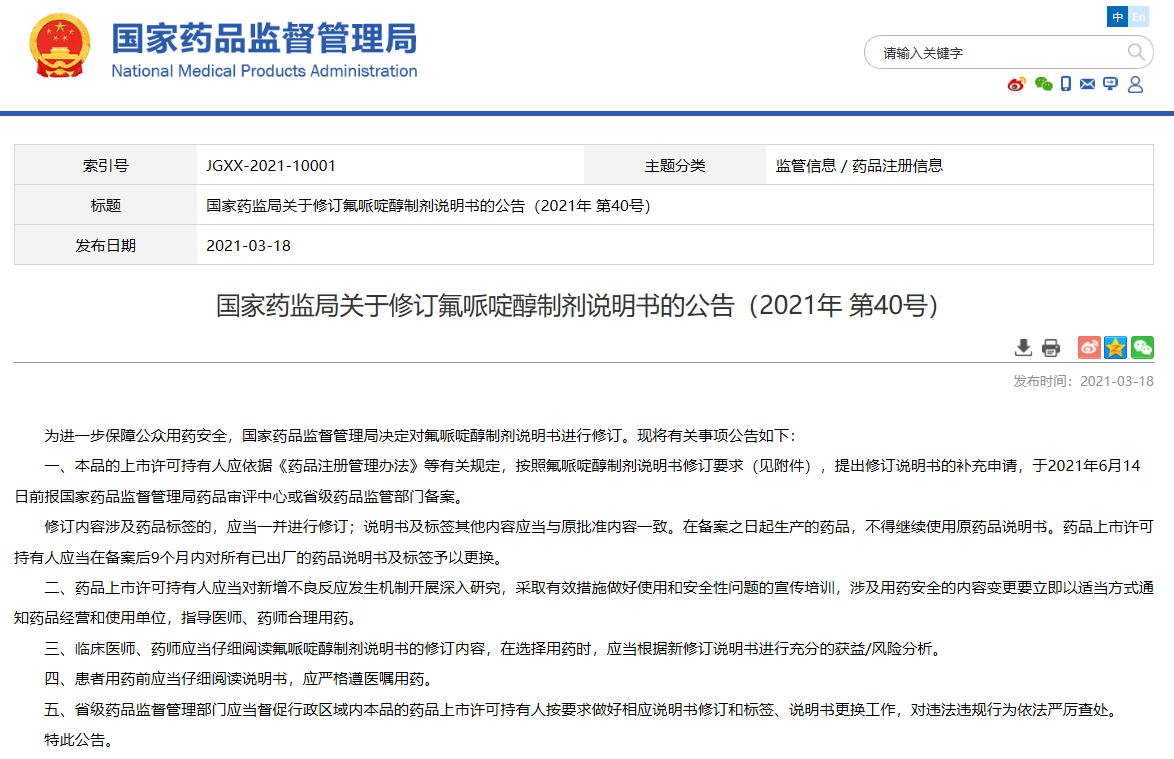
查看相关信息

关于发布《皮肤外用化学仿制药研究技术指导原则(试行)》的通告(2021年第23号)

查看相关信息

本周发布11个品种的国家药品标准公示。
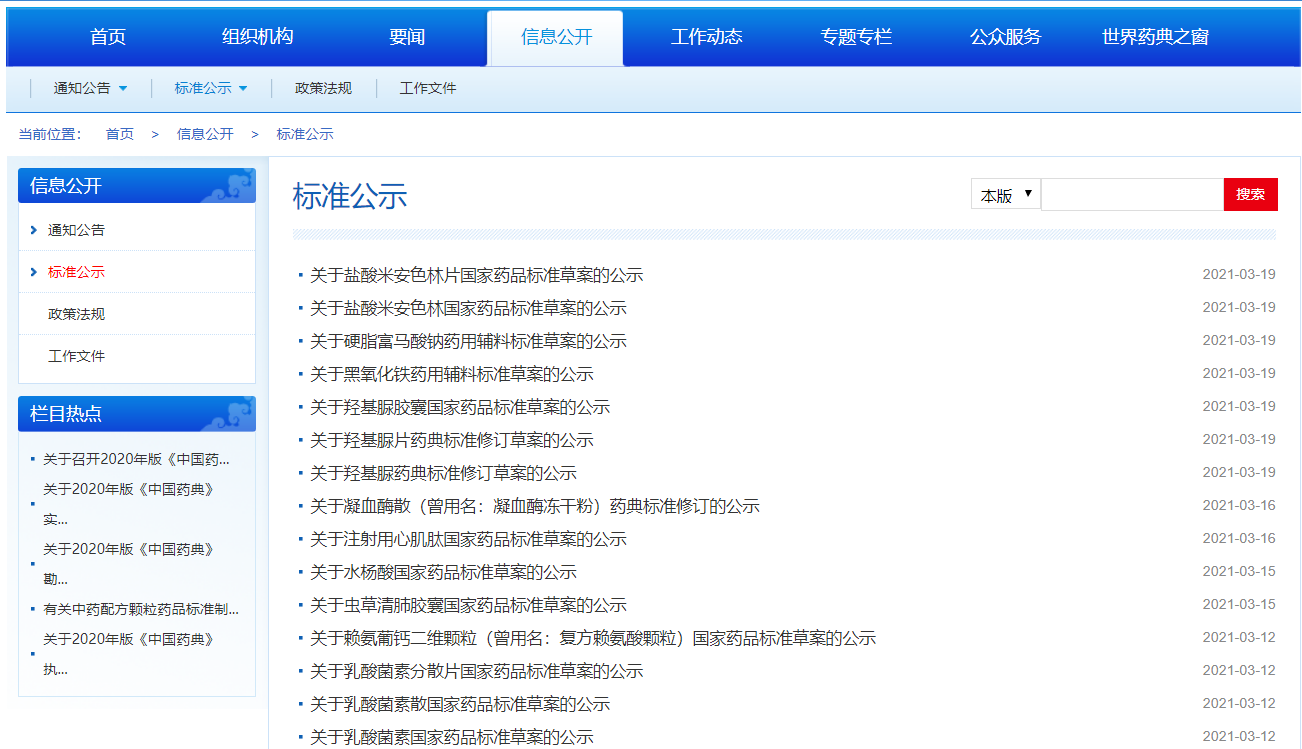
扫描下方二维码
查看相关信息

-END-
关于我们:
药政部是隶属于公司副总裁直接领导下的部门,以国家药品政策为导向,以为客户提供集药物研发、注册申报、现场核查等一体化专业技术服务为宗旨,以高效、成功申报项目最终目标。
药政部拥有一支技术与注册经验丰富的团队,作为一家提供专业服务的公司,在原料药登记、仿制药一致性评价、仿制药注册、新药注册以及进口药品注册等方面均具有专业且丰富的经验,已助力成功申报多项药品注册申请,在业内具有良好的口碑。
部门坚持 “忠诚、思考、建设、承担、分享”的公司理念,不断加强人才队伍建设、提升专业能力、丰富注册经验、拓展业务范围,致力于为客户提供高效率、高质量、合规的技术服务,为保护和促进公众健康而不懈努力。


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450