政策法规||本周重磅政策法规概览(21.05.17-21.05.21)
NMPA/CDE/CFDI/药典委公布药品相关内容本周集锦。
01
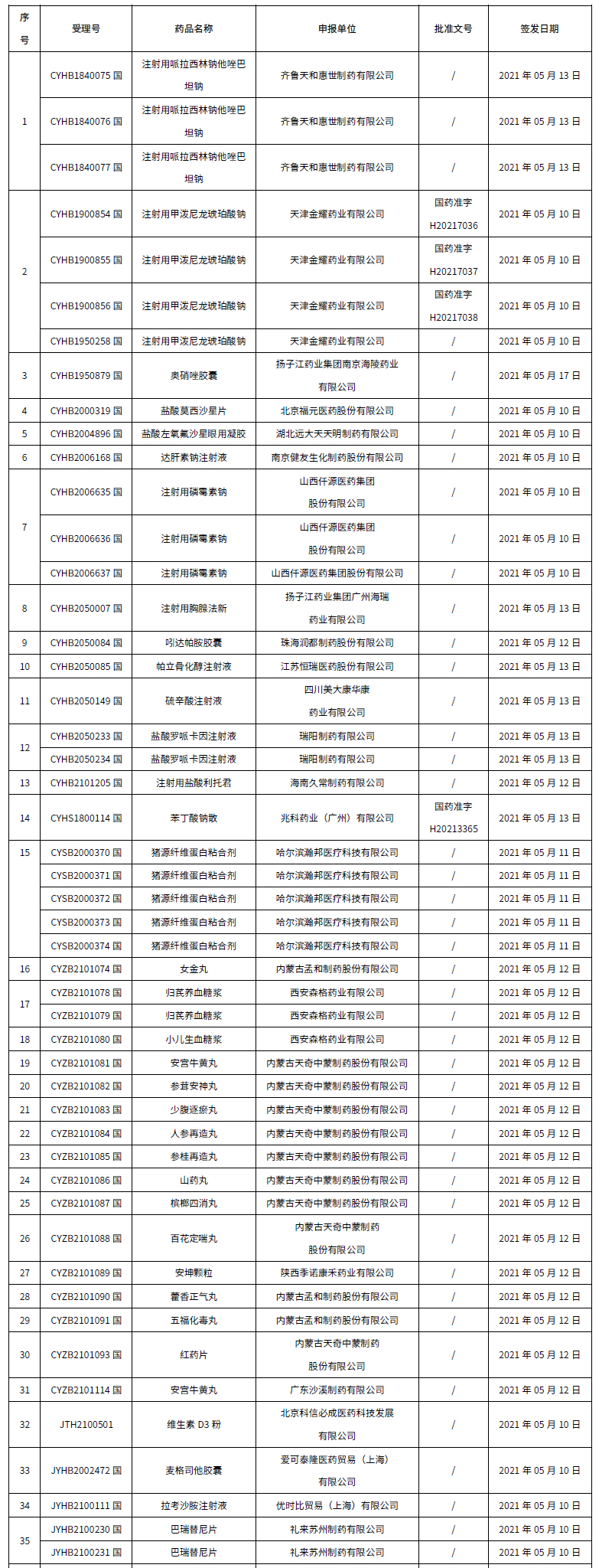
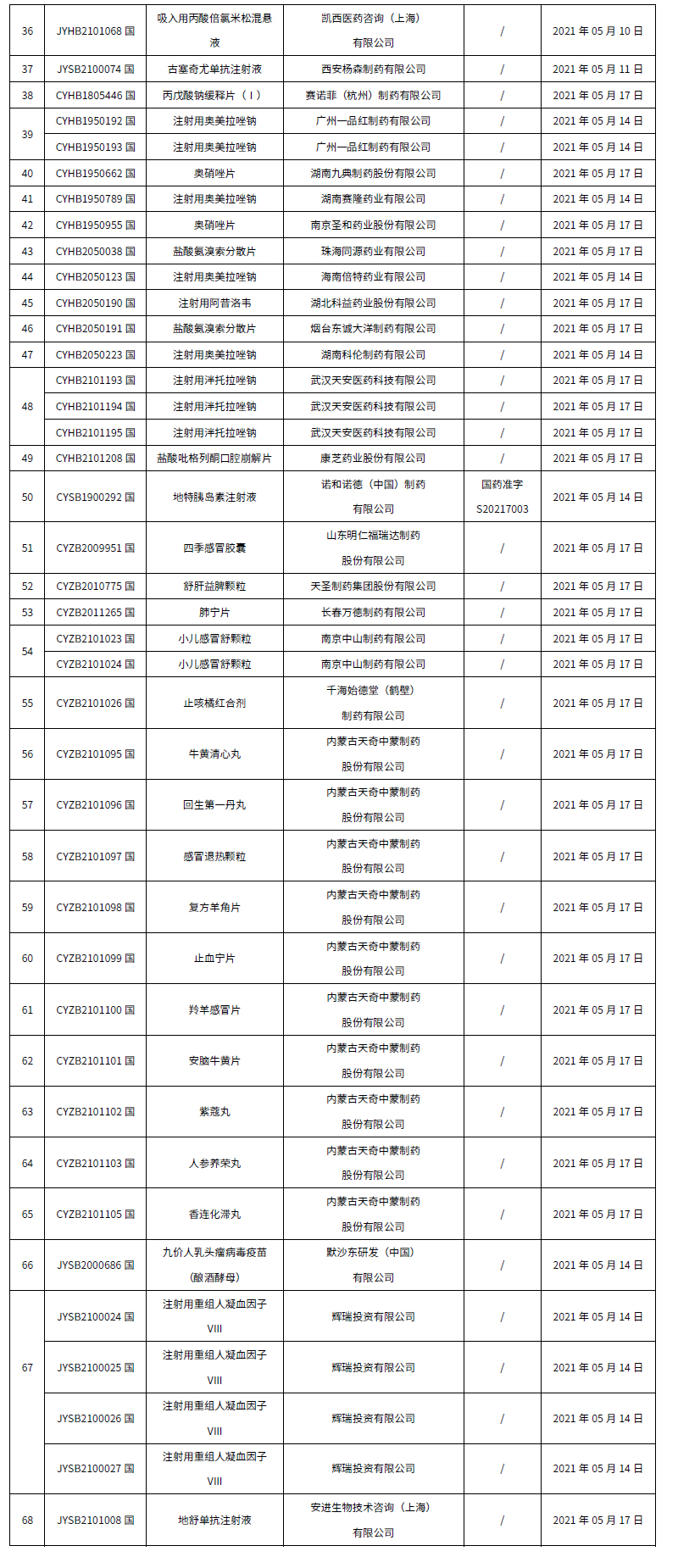
本周共计68个品种获批取得药品批准证明文件,其中一致性评价品种17个,包括注射剂品种11个。
国家药监局关于修订银杏达莫注射液说明书的公告(2021年第71号)
一、本品的上市许可持有人应依据《药品注册管理办法》等有关规定,按照银杏达莫注射液说明书修订要求(见附件),提出修订说明书的补充申请,于2021年8月19日前报国家药品监督管理局药品审评中心或省级药品监管部门备案。修订内容涉及药品标签的,应当一并进行修订;说明书及标签其他内容应当与原批准内容一致。在备案之日起生产的药品,不得继续使用原药品说明书。药品上市许可持有人应当在备案后9个月内对所有已出厂的药品说明书及标签予以更换。
二、药品上市许可持有人应当对新增不良反应发生机制开展深入研究,采取有效措施做好使用和安全性问题的宣传培训,涉及用药安全的内容变更要立即以适当方式通知药品经营和使用单位,指导医师、药师合理用药。
三、临床医师、药师应当仔细阅读银杏达莫注射液说明书的修订内容,在选择用药时,应当根据新修订说明书进行充分的获益/风险分析。
四、患者用药前应当仔细阅读说明书,应严格遵医嘱用药。
五、省级药品监督管理部门应当督促行政区域内本品的药品上市许可持有人按要求做好相应说明书修订和标签、说明书更换工作,对违法违规行为依法严厉查处。
扫描下方二维码
查看详细信息

01
关于发布《化学仿制药参比制剂目录(第四十三批)》的公示(征求意见稿)
本批公布共计40个品规的参比制剂来源;并且44个品种未通过审议,原因主要集中于安全有效性数据有限、经评价不具有参比制剂地位、规格不符合国内用法用量、拟申请参比制剂与已发布参比制剂浓度相同仅装量不同、改剂型未改变给药途径且无明显临床优势等。

扫描下方二维码
查看详细信息

关于发布《化学仿制药参比制剂目录(第四十四批)》的公示(征求意见稿)
本批公布共计59个品规的参比制剂来源,其中新增补40个;并且30个品种未通过审议,原因主要集中于原研进口参比制剂且可获得,拟申请参比制剂为美国或日本上市的仿制药、缺乏完整充分的安全有效性数据等。

扫描下方二维码
查看详细信息

关于药品专利纠纷早期解决机制相关专利信息登记平台公开测试等有关事宜的通知
为贯彻落实《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》以及《专利法》有关规定,国家药监局会同有关部门积极推进药品专利纠纷早期解决机制实施办法的制定和出台。为配合办法实施,根据国家药监局整体工作部署,经内部讨论和征询专家及相关部门意见,我中心搭建了中国上市药品专利信息登记平台,并附填表说明、专利声明公开模板。现对登记平台开展公开测试,并征集各方意见。

扫描下方二维码
查看详细信息

药品审评检查长三角分中心及大湾区分中心开始启动药品注册核查工作
2021年5月17日,国家药监局核查中心指导药品审评检查长三角分中心开始了首家药品注册生产现场核查。5月8日,药品审评检查大湾区分中心也已启动了首家药品注册核查。
核查中心就药品注册核查有关工作与药品审评检查长三角分中心及大湾区分中心开展进行了数次全面、充分的沟通交流。根据分中心实际情况,核查中心全程指导其建立了各类药品注册核查工作程序与标准。结合两个分中心对其当前资源与能力评估情况,将第一批9个位于长三角地区及5个位于大湾区的药品注册核查任务转对应分中心组织开展。核查中心对核查全过程进行指导,并协调国家药品检查员参与支持。相关任务调整事宜国家药监局核查中心已正式发文通知相关药品注册申请人。
扫描下方二维码
查看详细信息

本周去乙酰毛花苷、缬沙坦片、缬沙坦胶囊、吡拉西坦注射液、复方炉甘石眼膏、鹤蟾片国家药品标准草案公示;缬沙坦国家药品标准修订草案的公示;乌梅炭、蛇蜕、瓜蒌皮、丁香、决明子、炒决明子、莱菔子、蒲黄、生马钱子、盐菟丝子、菟丝子、水蛭、葶苈子、芫花、九香虫、炒九香虫全国中药饮片炮制规范品种草案公示。
扫描下方二维码
查看详细信息

-END-
关于我们:
药政部是隶属于公司副总裁直接领导下的部门,以国家药品政策为导向,以为客户提供集药物研发、注册申报、现场核查等一体化专业技术服务为宗旨,以高效、成功申报项目最终目标。
药政部拥有一支技术与注册经验丰富的团队,作为一家提供专业服务的公司,在原料药登记、仿制药一致性评价、仿制药注册、新药注册以及进口药品注册等方面均具有专业且丰富的经验,已助力成功申报多项药品注册申请,在业内具有良好的口碑。
部门坚持 “忠诚、思考、建设、承担、分享”的公司理念,不断加强人才队伍建设、提升专业能力、丰富注册经验、拓展业务范围,致力于为客户提供高效率、高质量、合规的技术服务,为保护和促进公众健康而不懈努力。


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450