一文盘点:CAR-T细胞在血液系统肿瘤的研究进展
世界上第一个CAR-T临床试验于2003年在美国启动,用于治疗上皮性卵巢癌。在中国,第一个CAR-T试验于2012年发布,旨在研究CD20靶向CAR-T细胞治疗化疗耐药或难治的淋巴瘤患者的可行性。
截止到2020年6月30日,中国已注册357个CAR -T临床试验,美国注册256个CAR-T临床试验,其他国家注册58个CAR-T临床试验。
在中国的357项临床试验中,有306项属于I期研究,有19项属于II期研究,有1项进入了III期研究(于2020年注册);在美国的256个临床试验中,I期、II期和III期试验的数量分别为209、25和4;在其他国家/地区的58项临床试验中,I期、II期和III期试验的数量分别为42、7和1[1]。
表1 FDA已经批准的CAR-T产品
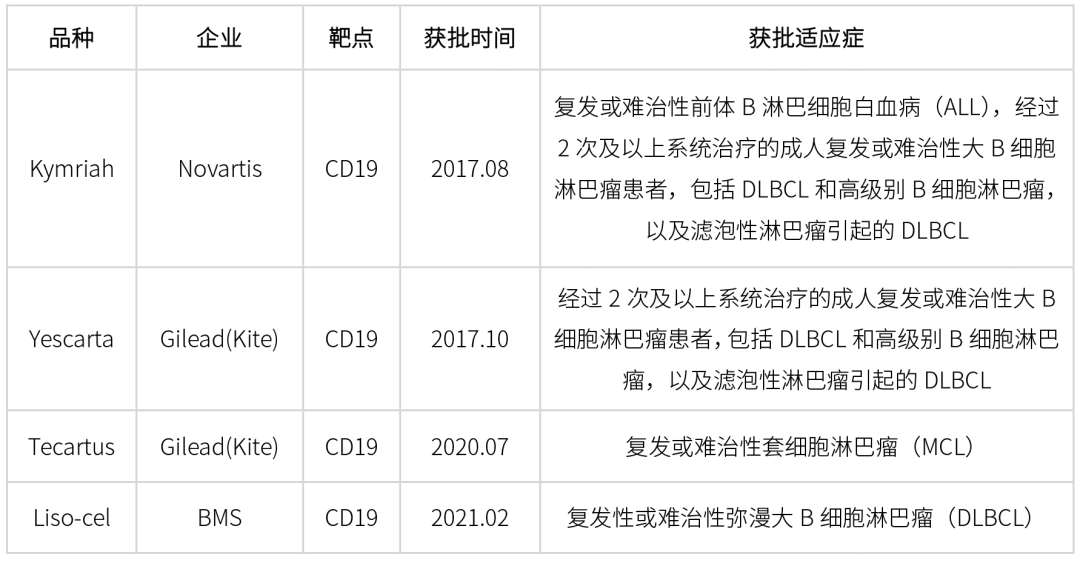
2021年1月12 日,NMPA显示,复星凯特CAR-T产品「阿基仑赛注射液」的上市申请(受理号:CXSS2000006)进入行政审批阶段,预计将在近日获批。这意味着国内首款 CAR-T 疗法产品即将获批上市。
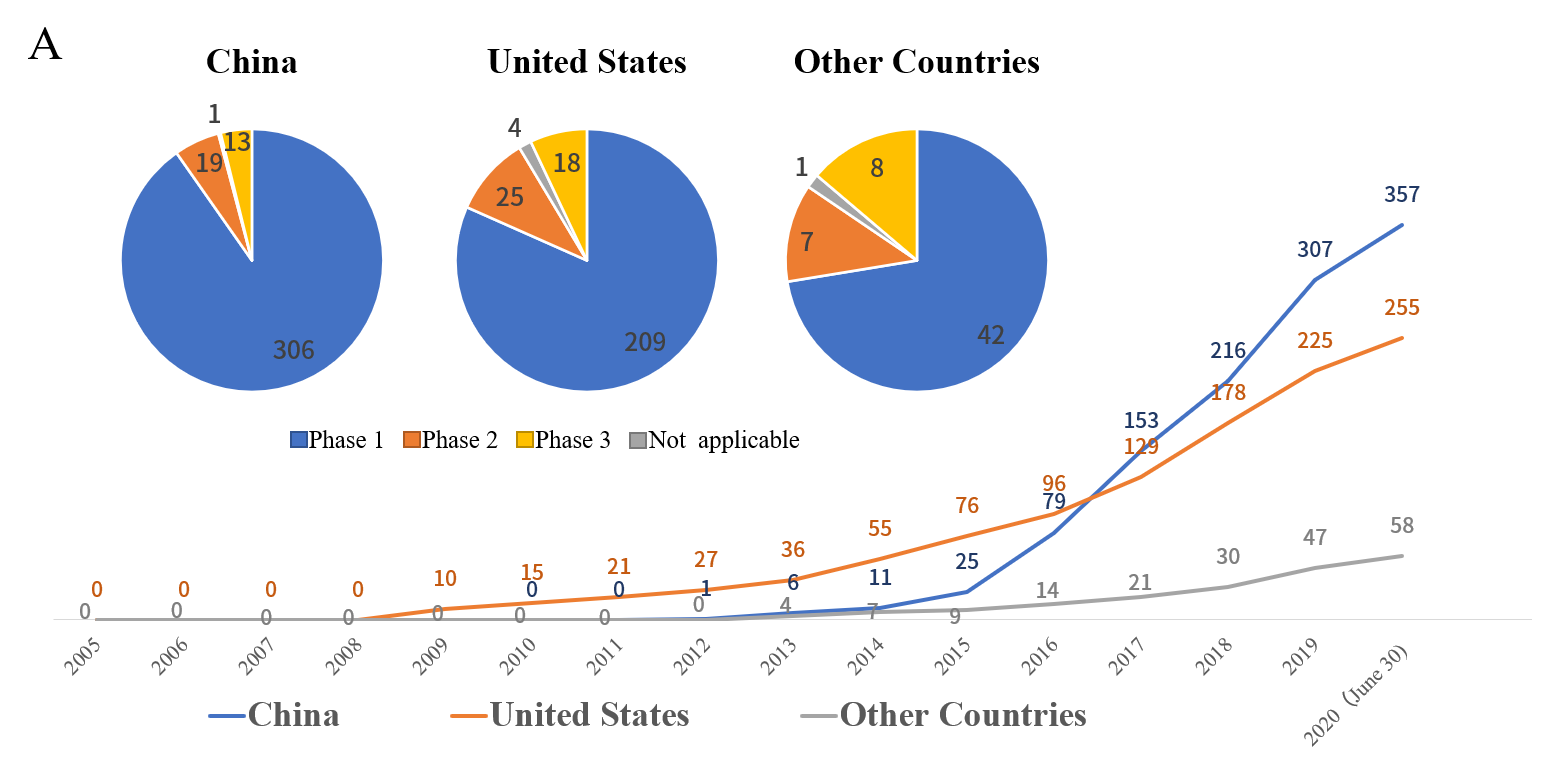
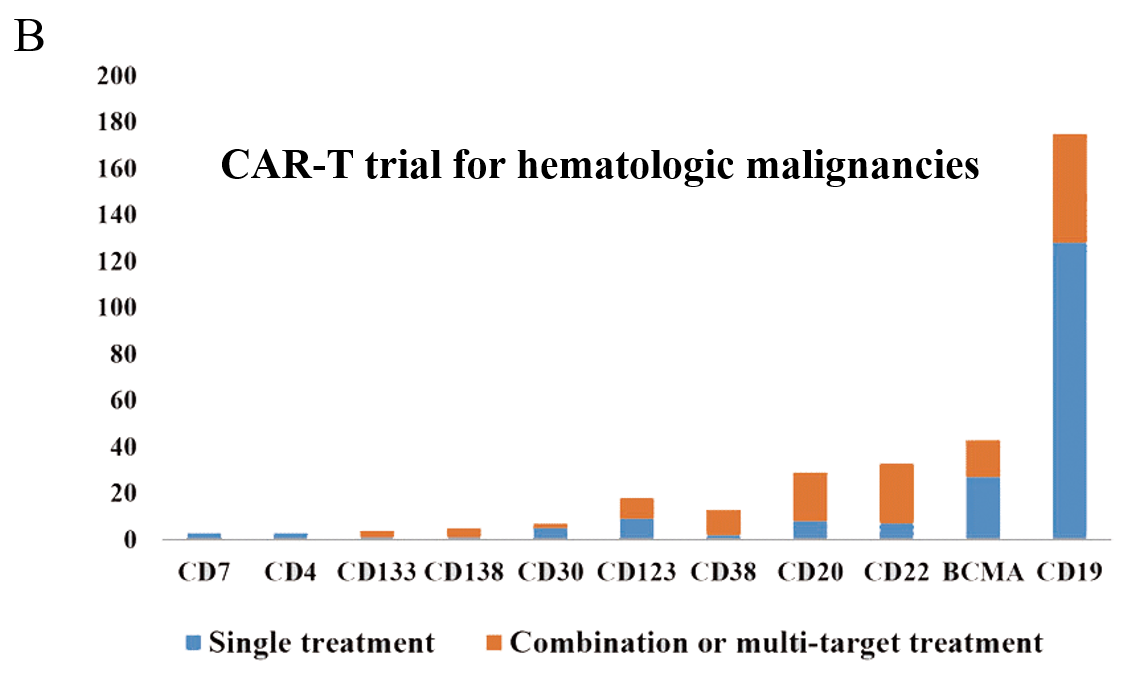
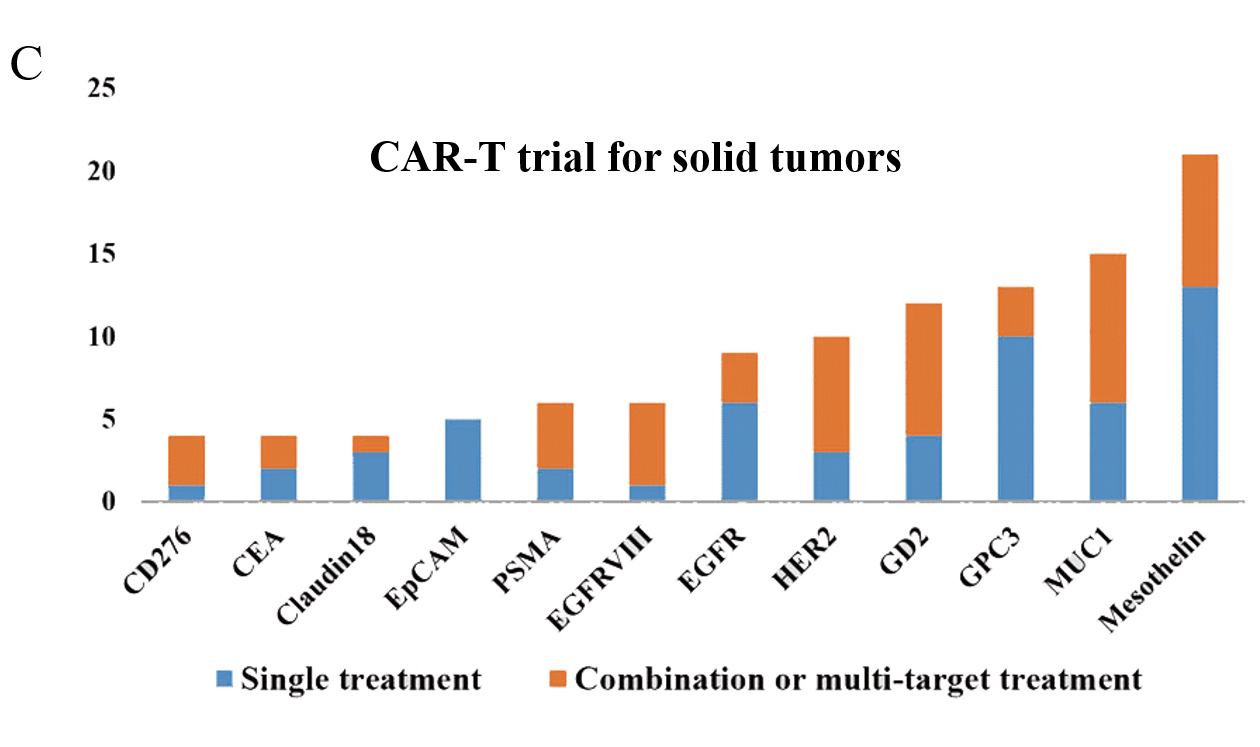
图1:每年注册CAR - T临床试验数量的变化和当前试验的阶段, 以及国内目前 CAR-T 细胞治疗在血液瘤、实体瘤中注册的临床试验项目数量[1]
CAR-T细胞组成:外周血分离的T细胞和通过基因工程设计的外源性嵌合抗原受体(chimeric antigen receptor, CAR)。
CAR的主要结构由肿瘤抗原受体和信号转导域组成。肿瘤抗原受体识别特定的肿瘤相关抗原,包括蛋白质,糖蛋白和其他元素,而信号转导域主要是增强T细胞的增殖和分化。
✎ 第一代CAR仅有一个T细胞受体(TCR)CD3ζ分子胞内信号域,然而,由于一代CAR-T细胞扩增慢和持久性差,在临床试验中疗效甚微;
✎ 第二代CAR包含一个共刺激域,其衍生自CD28或4-1BB结构域,在细胞增殖和衰老方面表现出显著的改善;
✎ 第三代在第二代的基础上强化了信号转导域中的另一种共刺激分子,第三代CAR同时包含两个不同的共刺激信号,例如CD28和CD137;
✎ 第四代CAR中添加了一些化学物质或细胞因子,其可以在肿瘤组织中分泌重要的化学物质或细胞因子,通过克服肿瘤微环境中的免疫抑制来提高对肿瘤细胞的毒性作用[2]。
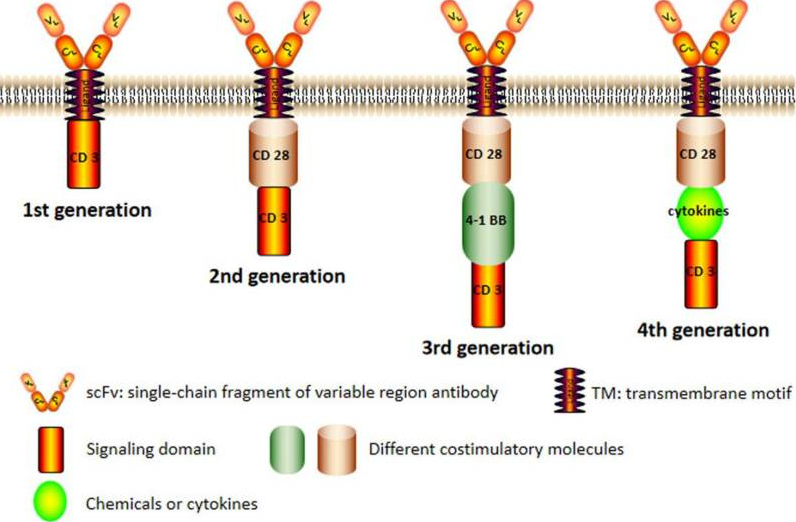
图2:四代嵌合抗原受体(CAR)的结构[2]
表2 CAR-T细胞治疗血液系统恶性肿瘤[2]
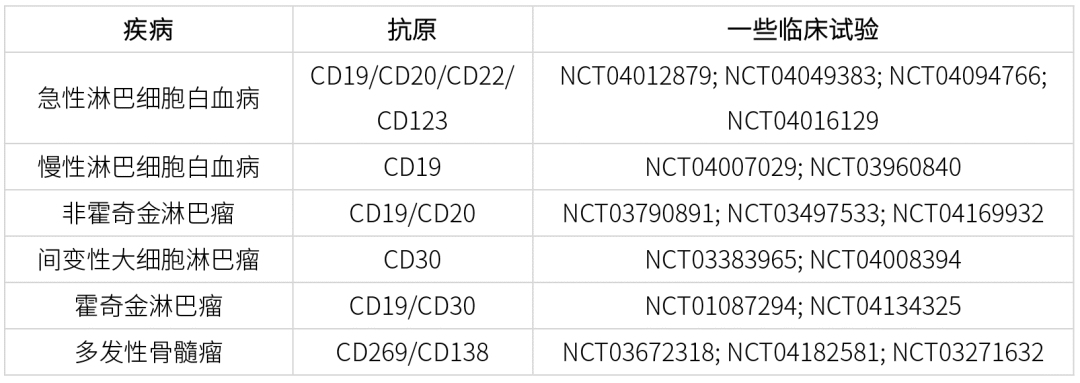
CAR-T细胞治疗可有效治愈急性淋巴细胞白血病(ALL),尤其适用于致命的复发或难治性B-ALL。CD19是B细胞的重要分子标志物,由于其在肿瘤细胞表面的较高表达,几乎是治疗B-ALL的理想靶标。诺华研发的Kymriah是一种CD19特异性CAR-T细胞药物,已获得FDA批准。
由于癌细胞的“抗原逃逸”,一些患者逐渐变得对CD19特异性CAR-T细胞不敏感[3]。幸运的是研究人员发现CD20、CD22、CD123等都可能称为潜在的靶标[4-5]。
慢性淋巴细胞性白血病(CLL)可能产生早期免疫缺陷,并导致比ALL更复杂的临床症状。常规治疗是同种异体干细胞移植联合化学疗法或放射疗法。近年来,研究人员开始探索CAR-T细胞在复发性和高风险CLL中的应用,其中CD19 CAR-T细胞是最常用的,一些临床试验显示出了良好的疗效。
包括非霍奇金淋巴瘤(NHL),间变性大细胞淋巴瘤(ALCL),霍奇金淋巴瘤(HL)在内的淋巴瘤最传统的治疗方法是化疗方案和单克隆抗体。上述药物在一定程度上显示出临床成功,但仍有一些患者在这些疗法后出现了疾病恶化。必须有一种新颖有效的淋巴瘤疗法,CAR-T细胞可用于治疗顽固性B细胞淋巴瘤或预后较差的患者。
研究调查了CD19 CAR-T细胞对淋巴瘤患者的效率,并显示出令人鼓舞的结果,即75%的患者达到PR[6]。除CD19外,CD20或CD30在CAR-T细胞治疗淋巴瘤方面也必不可少。
多发性骨髓瘤(MM)是一种难治性血液系统肿瘤,其特征是浆细胞融合在骨髓中,可导致贫血,免疫抑制,高钙血症,骨病变和肾功能衰竭。
虽然抗CD19 CAR-T细胞治疗在治疗其他血液学恶性肿瘤方面表现出色,但由于骨髓瘤细胞表面CD19表达较低,因此不能表现出良好的清除骨髓瘤细胞的效果。CD269 (BCMA)分子主要在成熟B细胞或浆细胞中表达,是多发性骨髓瘤的一个很有前途的靶点[7]。另一个参与的分子CD138,它在恶性浆细胞上表达。临床试验表明,CD138 CAR-T细胞经输注后进入骨髓,具有潜在的抗肿瘤免疫作用,且无不可耐受的毒性。在基础研究结束后,还需要进一步探索肿瘤细胞呈现出更明确的靶点,进行更多的临床试验。
CAR-T细胞治疗为血液系统恶性肿瘤患者的治疗提供了广阔的前景, 为开发其他癌症的治疗策略奠定了基础。但如何提高 CAR-T 细胞的靶向性、抗肿瘤作用;如何减少和改善不良反应,提高生存率,仍是 CAR-T治疗的重点和难点。随着基因编辑技术的日益精确以及治疗方案的持续断优化,CAR-T 治疗将不断得到完善和改进。
参考文献
[1] Wei J , Guo Y , Wang Y , et al. Clinical development of CAR T cell therapy in China: 2020 update[J]. Cellular & Molecular Immunology, 2020:1-13.
[2] Han D, Xu Z, Zhuang Y, Ye Z, Qian Q. Current Progress in CAR-T Cell Therapy for Hematological Malignancies. J Cancer. 2021;12(2):326-334. Published 2021 Jan 1. doi:10.7150/jca.48976
[3] Eugenia, Zah, Meng-Yin, et al. ADDENDUM: T Cells Expressing CD19/CD20 Bispecific Chimeric Antigen Receptors Prevent Antigen Escape by Malignant B Cells.[J]. Cancer Immunology Research, 2016.
[4] Matsueda S, Chodon T, Koya RC. Cellular Immunotherapy in the Treatment of Hematopoietic Malignancies. Adv Exp Med Biol. 2019;1143:217-229. doi: 10.1007/978-981-13-7342-8_10. PMID: 31338822.
[5] Pemmaraju, Naveen. Novel Pathways and Potential Therapeutic Strategies for Blastic Plasmacytoid Dendritic Cell Neoplasm (BPDCN): CD123 and Beyond[J]. Current Hematologic Malignancy Reports, 2017.
[6] Kochenderfer JN, Wilson WH, Janik JE, et al. Eradication of B-lineage cells and regression of lymphoma in a patient treated with autologous T cells genetically engineered to recognize CD19. Blood. 2010;116(20):4099-4102. doi:10.1182/blood-2010-04-281931
[7] Carpenter RO, Evbuomwan MO, Pittaluga S, et al. B-cell maturation antigen is a promising target for adoptive T-cell therapy of multiple myeloma. Clin Cancer Res. 2013;19(8):2048-2060. doi:10.1158/1078-0432.CCR-12-2422
-END-
关于我们:
郑州深蓝海生物医药是北京新领先在临床CRO领域打造的一个知名品牌。公司拥有300余人高专业水准的临床服务团队,并在石家庄、武汉、长沙、杭州、郑州、沈阳、贵州、大连、广州、西安等20多个中心城市设立驻地办事处。
公司下设医学部、临床运营部、数据部、质量控制委员会、药物警戒部、注册部和人类遗传资源管理委员会等部门。能够通过创新的服务模式和多维的信息化技术,推动临床研究的发展及临床研究外包服务模式的变革,为客户提供多元化的研发支持和服务,包括创新药和仿制药的Ⅰ~Ⅳ期临床试验、仿制药生物等效性(BE)试验及药代动力学(PK/PD)临床研究、体内外相关性研究(IVIVR)、医疗器械临床研究及第三方稽查等,全面覆盖大小分子药物,满足不同类型企业的临床研究需求,为国内外客户打通新药上市前最关键的瓶颈。
目前,公司已经与国内近1000家药物临床机构、600余家临床医院建立合作,如北京大学第一医院、北京安贞医院、北京阜外心血管医院、上海长海医院、复旦大学附属中山医院、江苏省人民医院、吉林大学中日联谊医院、哈尔滨医科大学附属第一医院、广东中医院、天津中医药大学附属第一医院等,合作医院科室1500余个。


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450