政策法规||中国新药注册临床试验进展年度报告(2021年)发布(附本周法规概览06.06-06.10)
发布时间:2022-06-10
国家药监局药审中心发布《中国新药注册临床试验进展年度报告(2021年)》
本次年度报告主要根据2021年度登记的药物临床试验信息,从药物类型、品种及靶点特征、适应症、申办者类型、注册分类、试验分类、试验分期、特殊人群试验、临床试验组长单位、启动耗时和完成情况等角度对临床试验的总体趋势变化、主要特点、突出问题等进行汇总分析,同时对比近三年临床试验登记数据,对近年来的趋势特征进行总结分析。

扫码识别图中二维码
查看详细信息

CDE
国家药监局药审中心关于发布《罕见疾病药物临床研究统计学指导原则(试行)》的通告(2022年第33号)

扫码识别图中二维码
查看详细信息

NMPA
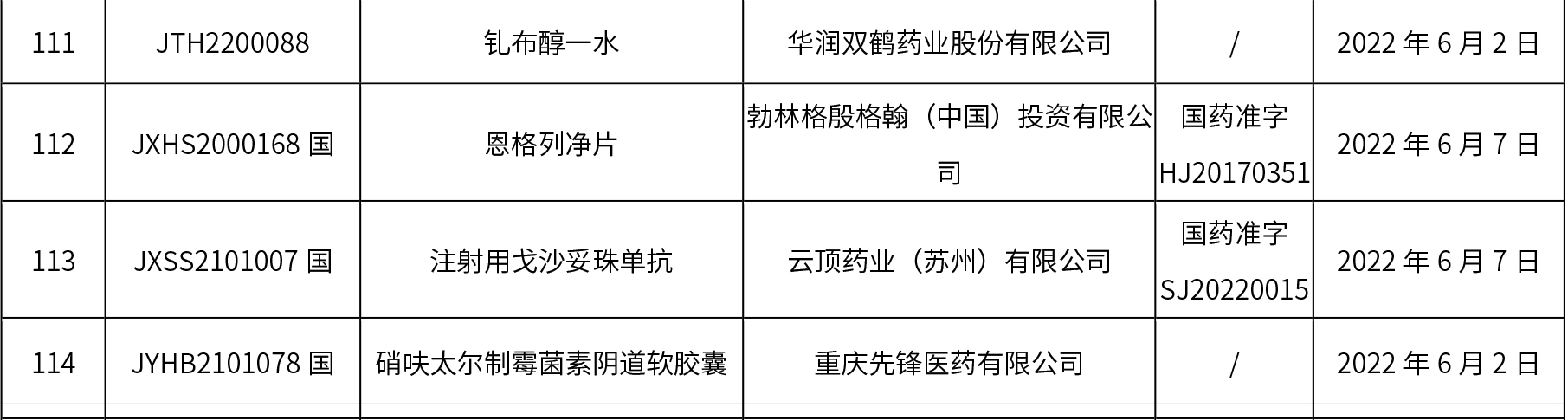
1、本周共发布了114个品规的药品批准证明文件待领取信息,其中一致性评价10个,注射剂48个。
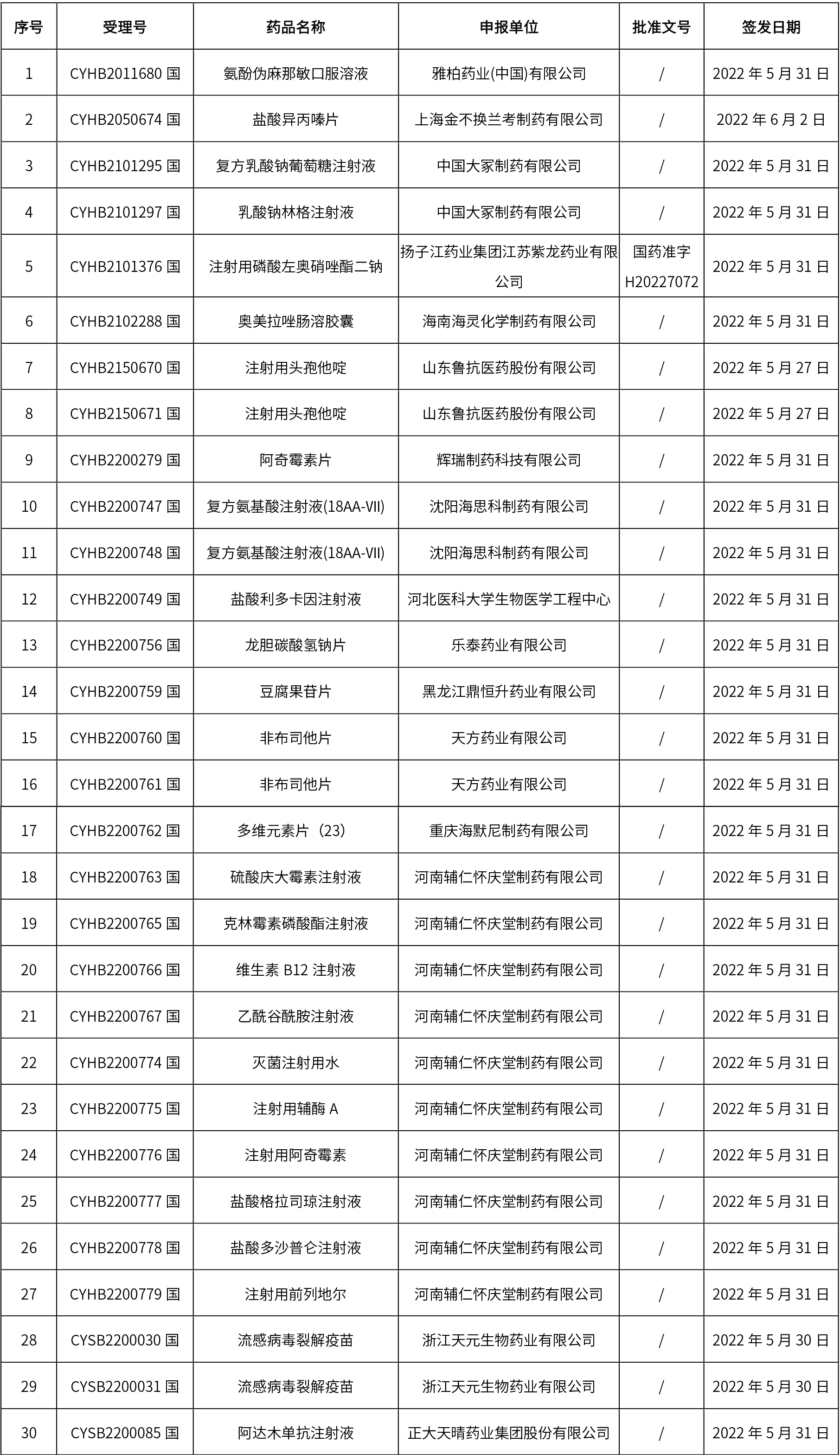
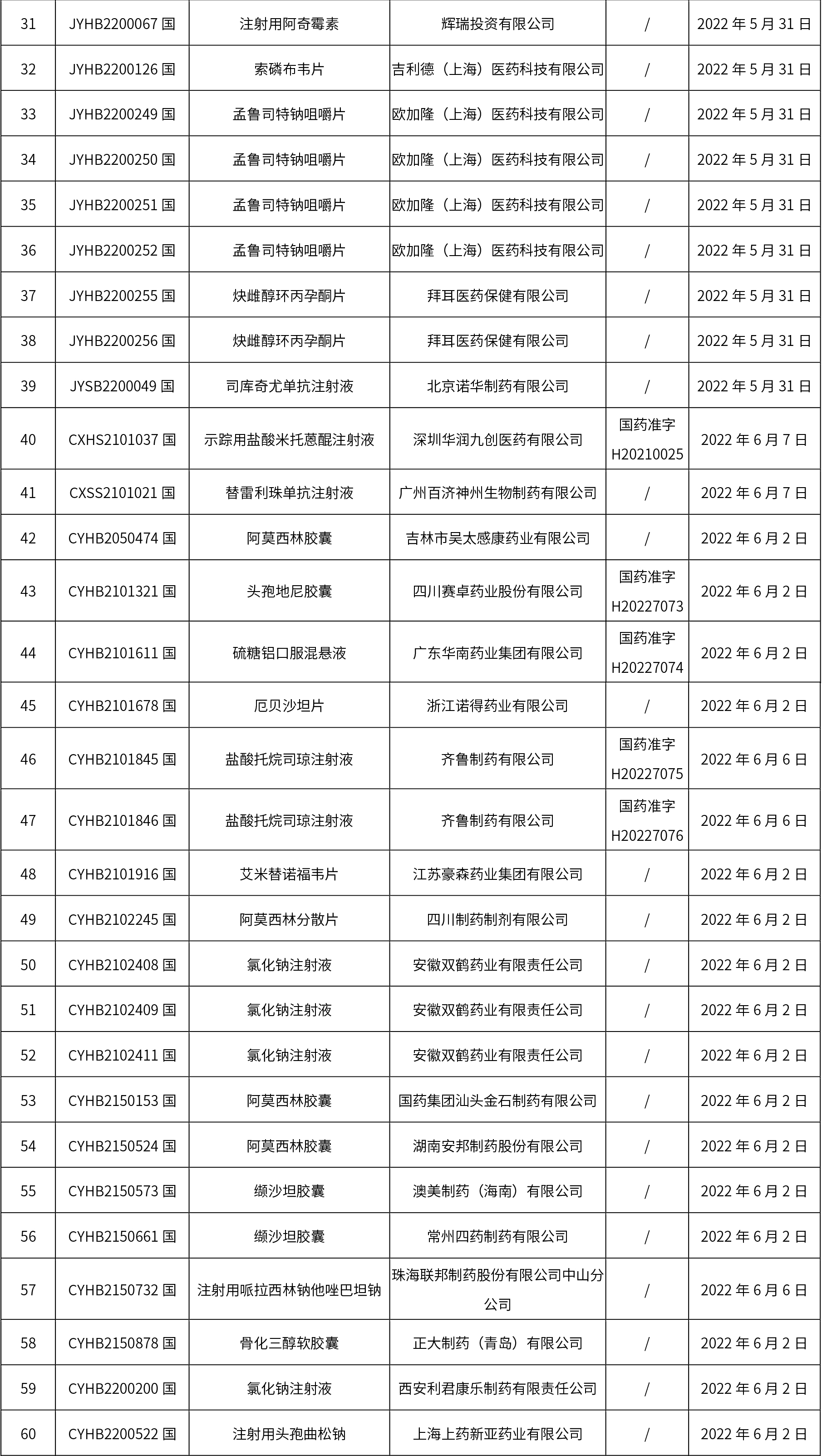
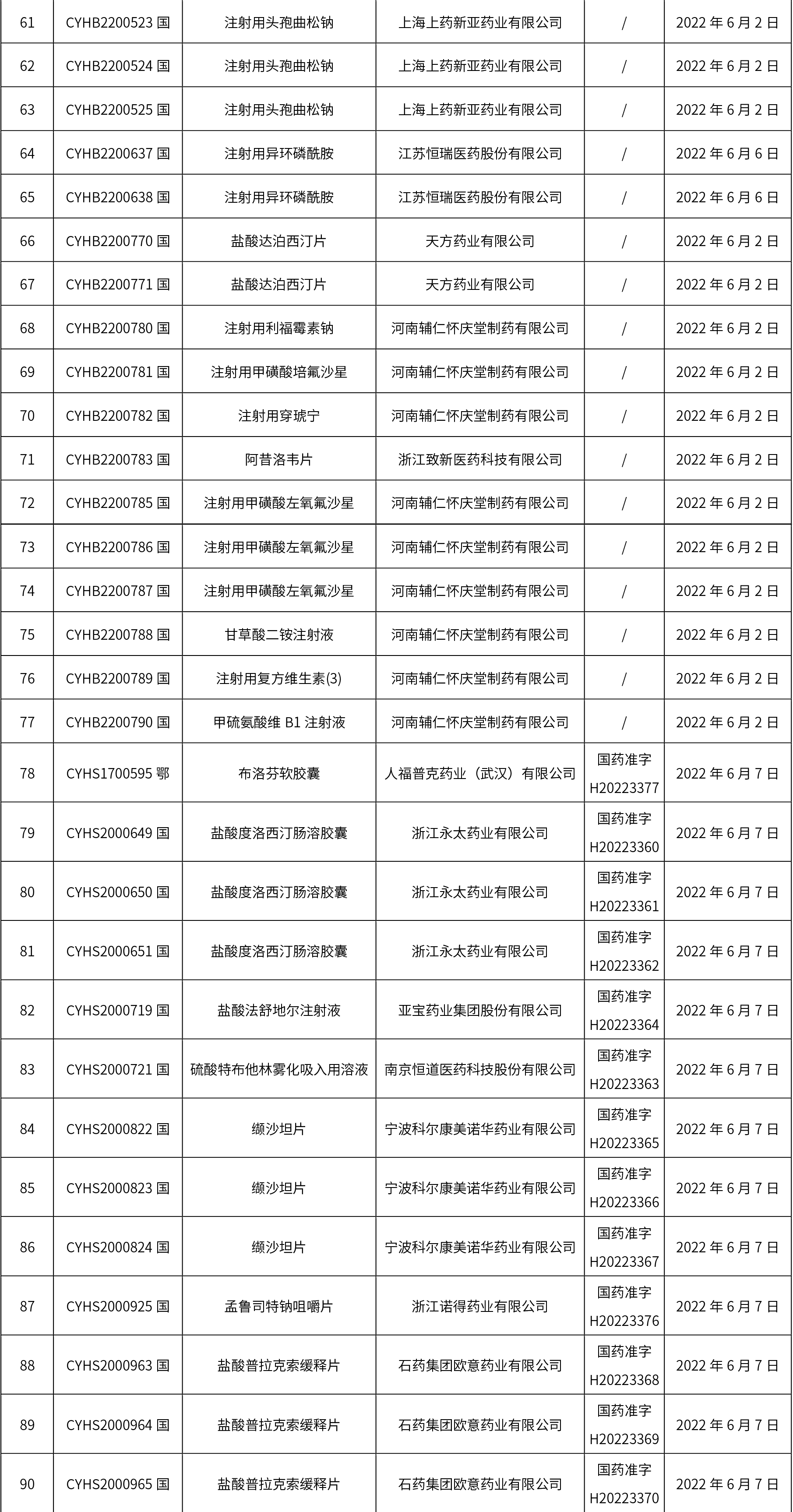
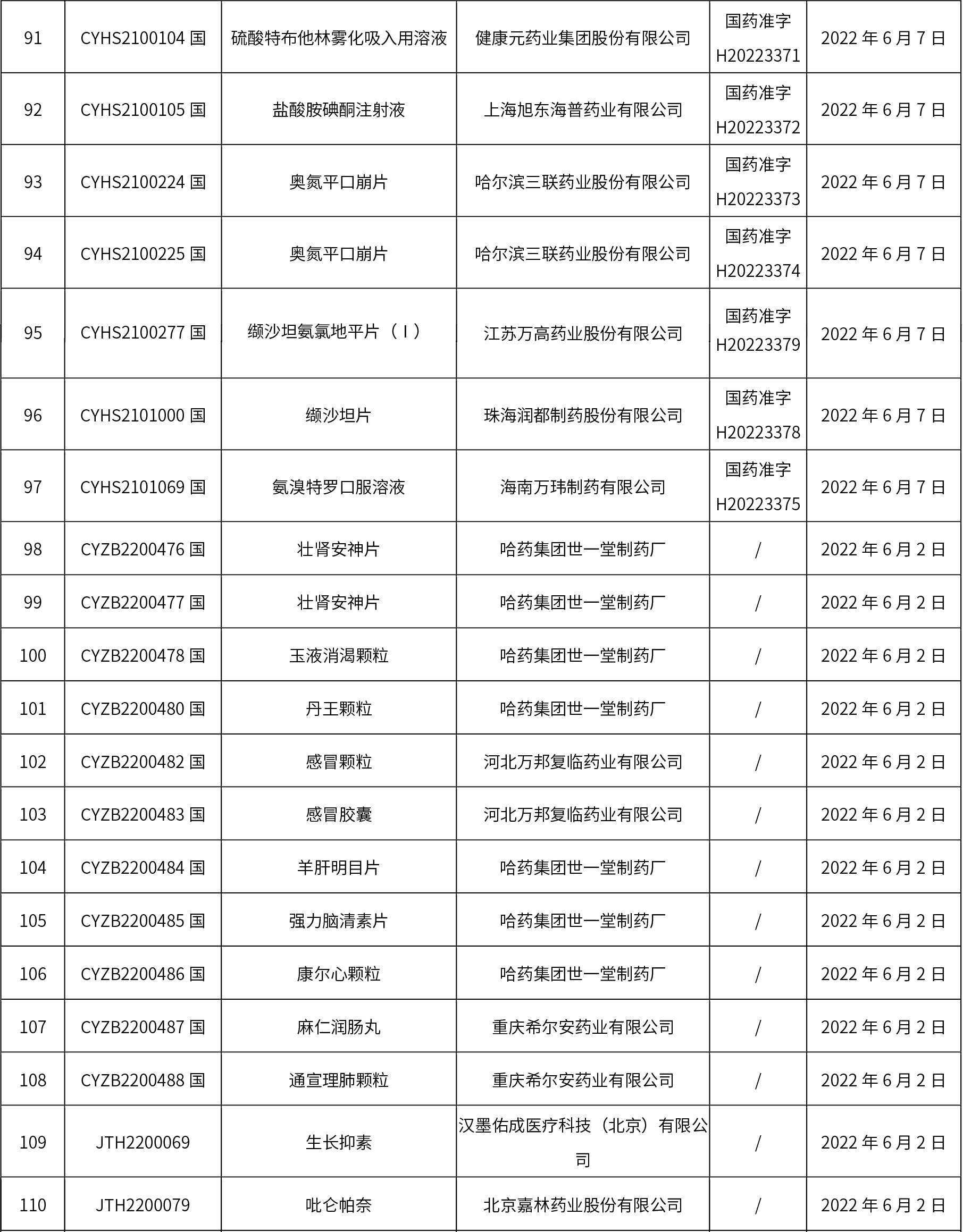
药典委
关于征求《中国药典》药包材生物学评价与试验选择指导原则意见的通知
扫码识别图中二维码
查看详细信息

-END-



转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450