汇总 | 国内外药品试验数据保护制度(附国内外数据保护制度对比图)
美国是最早对药品试验数据进行独占保护的国家。在Hatch-Waxman法案出台前,无论是新药上市申请(NDA)还是仿制药上市申请(ANDA),均必须向FDA提交临床试验数据。
1985年,Hatch-Waxman法案规定仿制药企业在申请仿制药上市时无需提交证明药品安全性和有效性的试验数据,只需要提交证明仿制药与原研药具有生物等效性的数据。
根据2004/27/EC号指令,欧盟目前对新药采取“8+2+1”的保护模式,即新药自获准上市之日起10年内受数据独占保护;在新药获准上市的前8年,药监部门不受理仿制药上市申请;在新药获准上市满8年后,药监部门可以受理仿制药上市申请,但在保护期届满前2年不批准仿制药上市;在8年“不受理”期间提出新适应症,延长1年保护期。
1979年修订的《药事法》规定了药品上市后的再审查制度。再审查制度是指新药在获得上市批准后的规定期限内,新药企业需要提交药品使用过程中的临床数据,供药监部门对新药在使用过程中的安全性和有效性进行审核。
《药事法》规定,药品数据保护制度的运行操作与再审查制度同步,再审查期即药品试验数据保护期。在保护期内,药监部门不受理仿制药上市申请。当试验数据保护期结束后,只需要审查仿制药是否与新药具有生物等效性即可
药品数据保护期限:
含新化学成分药品:8年
新医疗用配合剂或者新给药途径药物:6年
罕见病用药的:10年
新适应症、新剂量药物:4-6年
加拿大数据保护制度针对创新药,具有新适应症、新剂型的药品补充申请则无法获得保护。
创新药独占保护期为8年,采用“6+2”的保护模式,在独占保护期的前6年,仿制药企业不得提出上市申请,6年期满后可申请仿制药上市,但药监部门在保护期届满后方可批准仿制药上市。另外,创新药品如能够证明对儿童有治疗效果,则可以额外获得6个月的保护期。
我国药品数据保护制度建立历程:
· 对批准生产的新药品种设立监测期。监测期自新药批准生产之日起计算,最长不得超过5年。监测期内的新药,国家食品药品监督管理局不批准其他企业生产、改变剂型和进口。
· 对于已申请中药品种保护的,自中药品种保护申请受理之日起至作出行政决定期间,暂停受理同品种的仿制药申请。
我国采用市场独占的方式,根据药物的创新程度以及临床需求情况予以区分,创仿不能实现均衡发展。此外,目前的政策完全将专利链接制度与数据保护制度割裂开来,但二者有待衔接,如首仿专利挑战,专利挑战成功后即可批准上市,但原研药品仍可能在数据保护期内。
相信随着专利链接制度落地以及《药品管理法实施条例》的修订,我国的数据保护制度将会很快正式出台实施。
国内外数据保护制度对比图
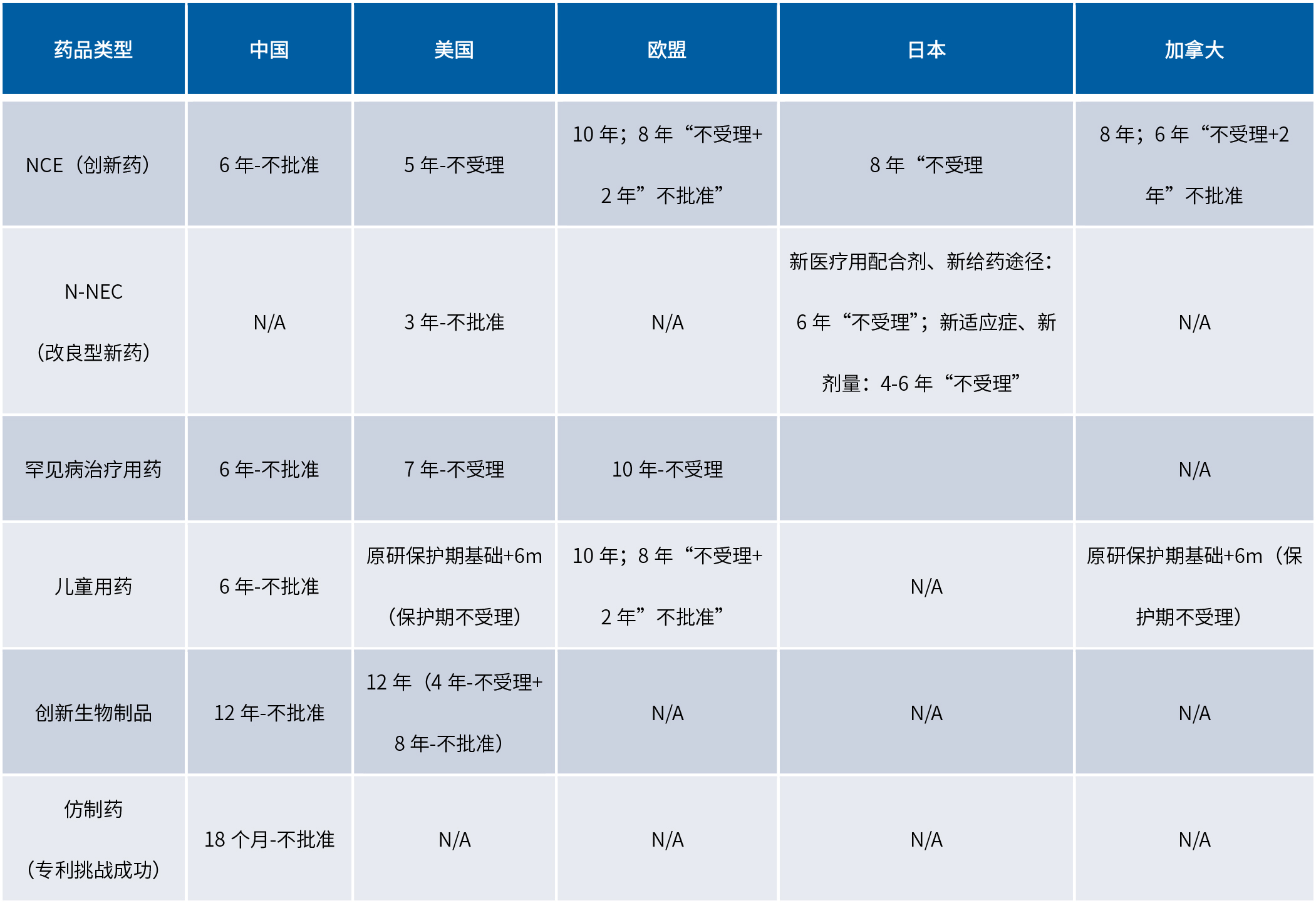
(点击查看大图)
-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450