政策法规||国家药监局发布《药物警戒检查指导原则》(附本周法规概览04.11-04.15)
发布时间:2022-04-15
本周热点
01
国家药监局关于印发《药物警戒检查指导原则》的通知
为落实《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》有关建立药物警戒制度的要求,指导药品监督管理部门科学规范开展药物警戒检查工作,国家药监局组织制定了《药物警戒检查指导原则》。
长按识别图中二维码
查看详细信息

02
关于公开征求《双特异性抗体类抗肿瘤药物临床研发技术指导原则》意见的通知
为了对双特异性抗体类抗肿瘤药物的临床研发中,需要特殊关注的问题提出建议,并指导企业开展更为科学的临床研发,药品审评中心组织撰写了《双特异性抗体类抗肿瘤药物临床研发技术指导原则》,形成征求意见稿,供药物研发相关人员参考。

长按识别图中二维码
查看详细信息

本周法规盘点
NMPA
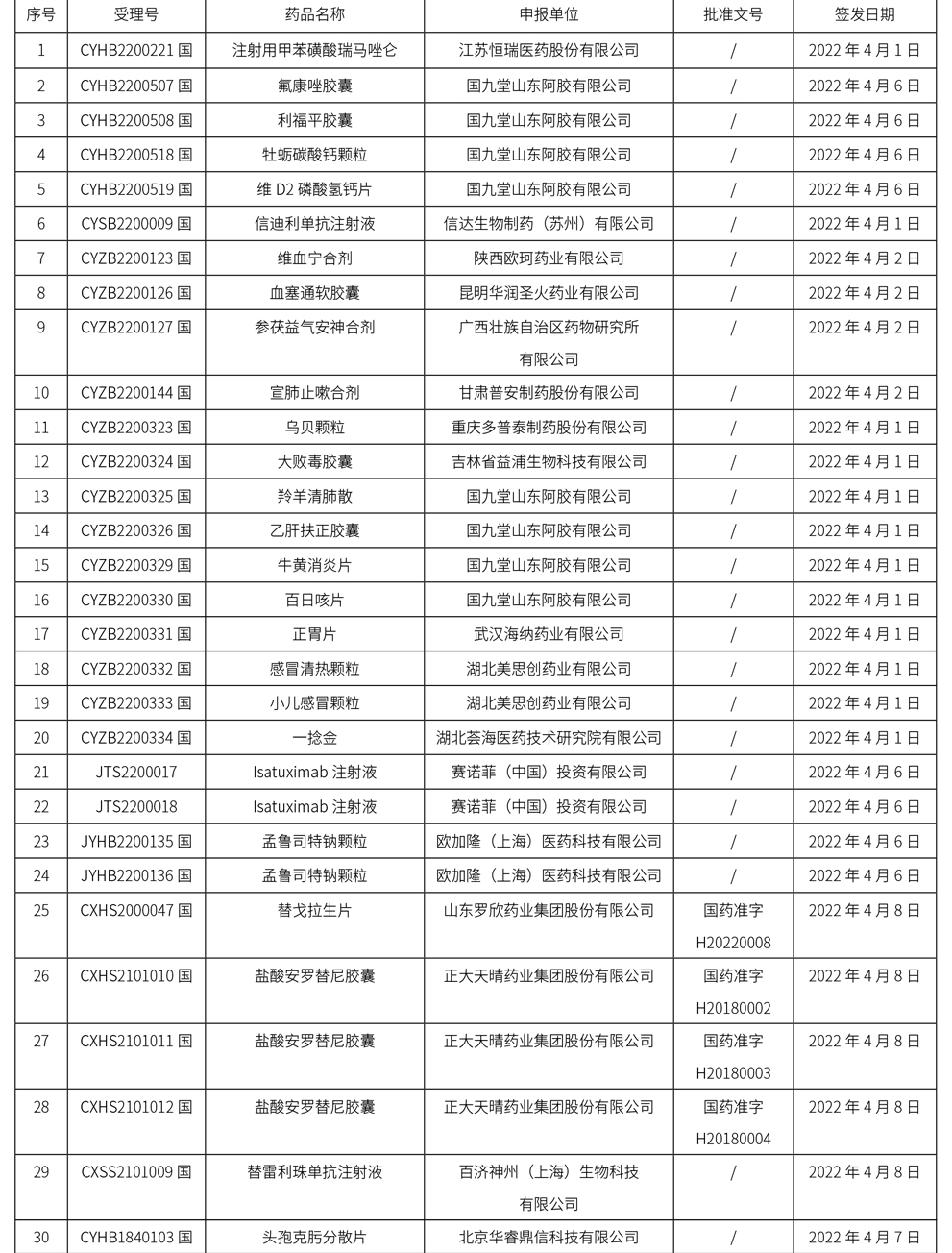
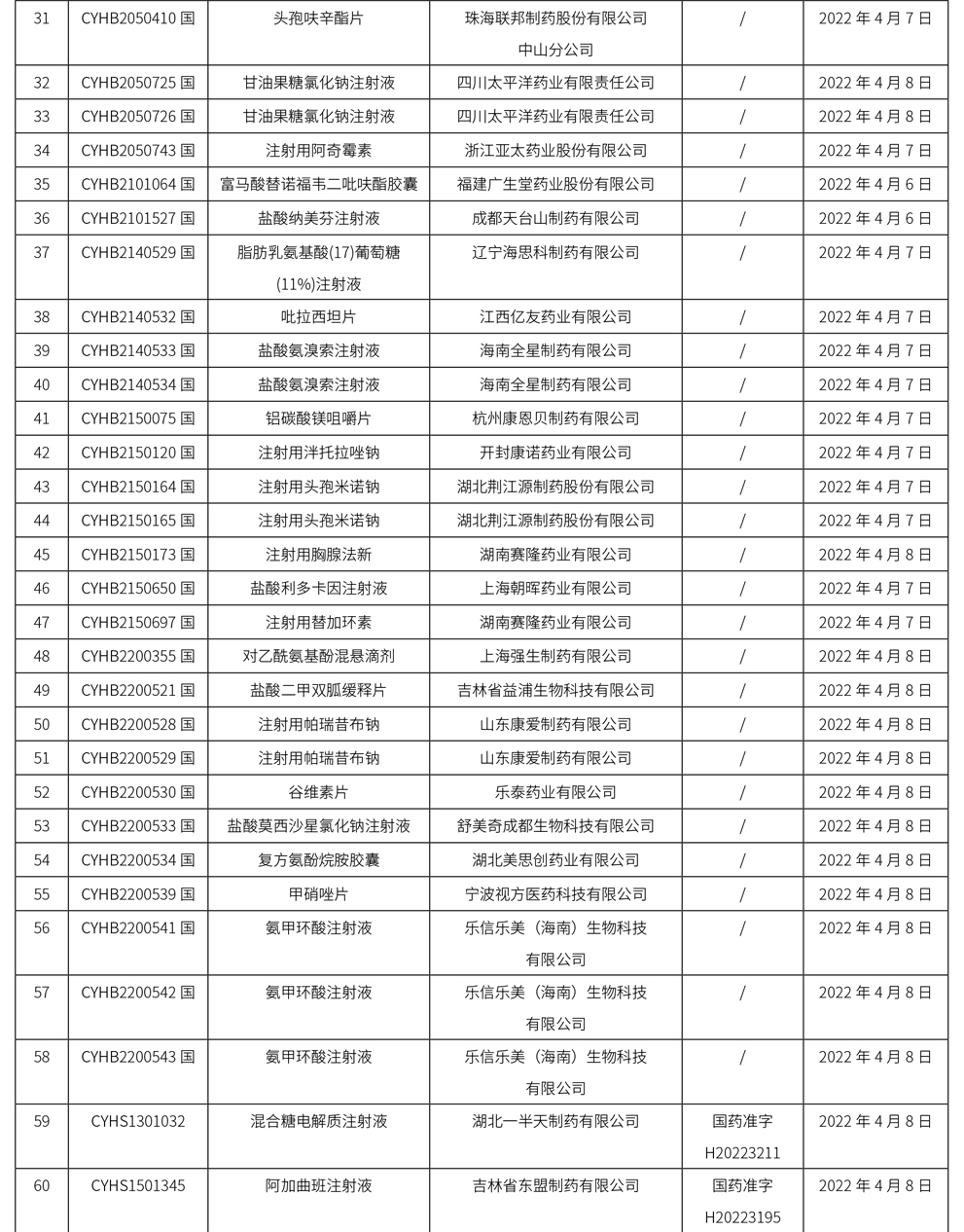
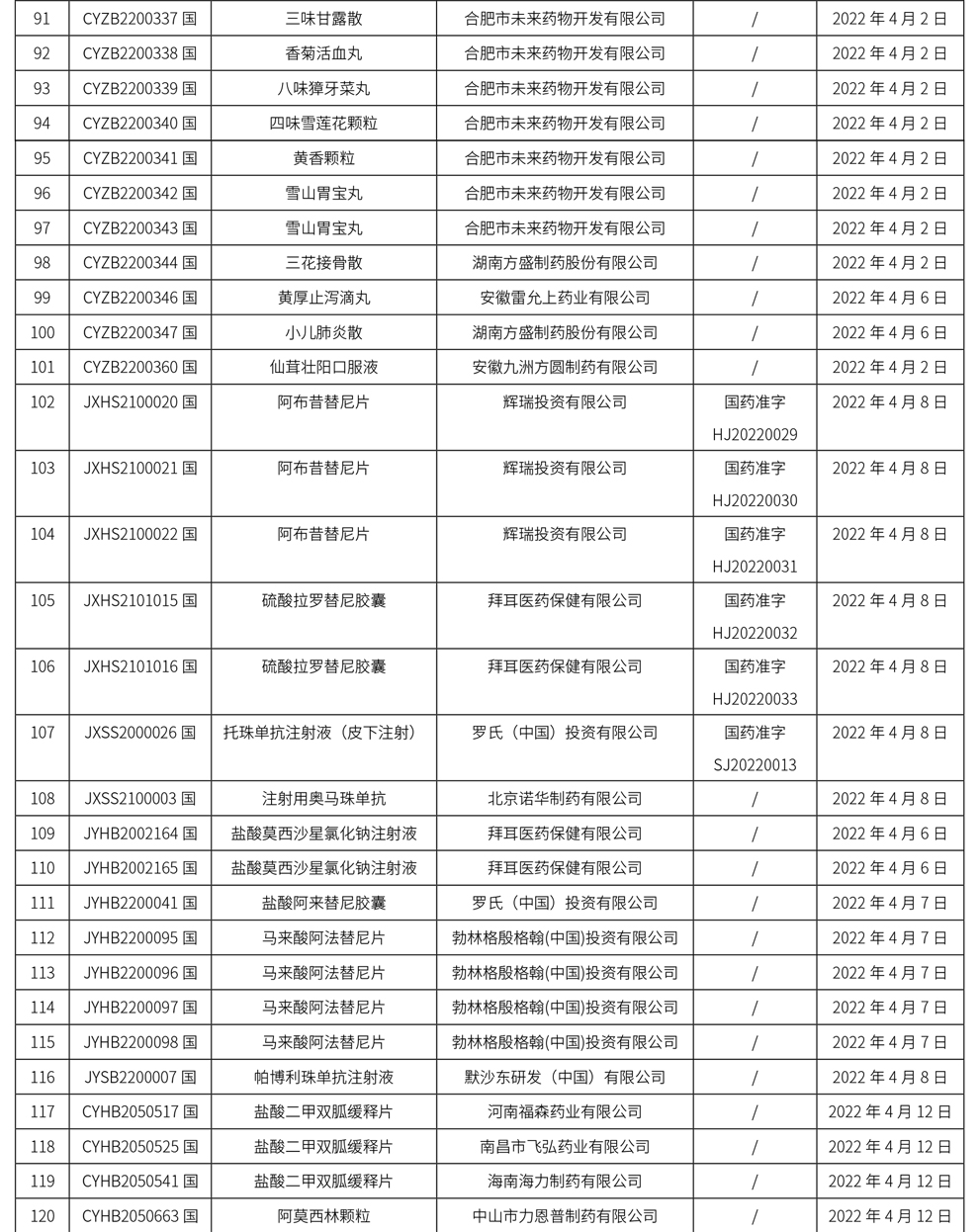
1、本周共计175个品种取得药品批准证明文件,其中一致性评价品种26个,注射剂72个。

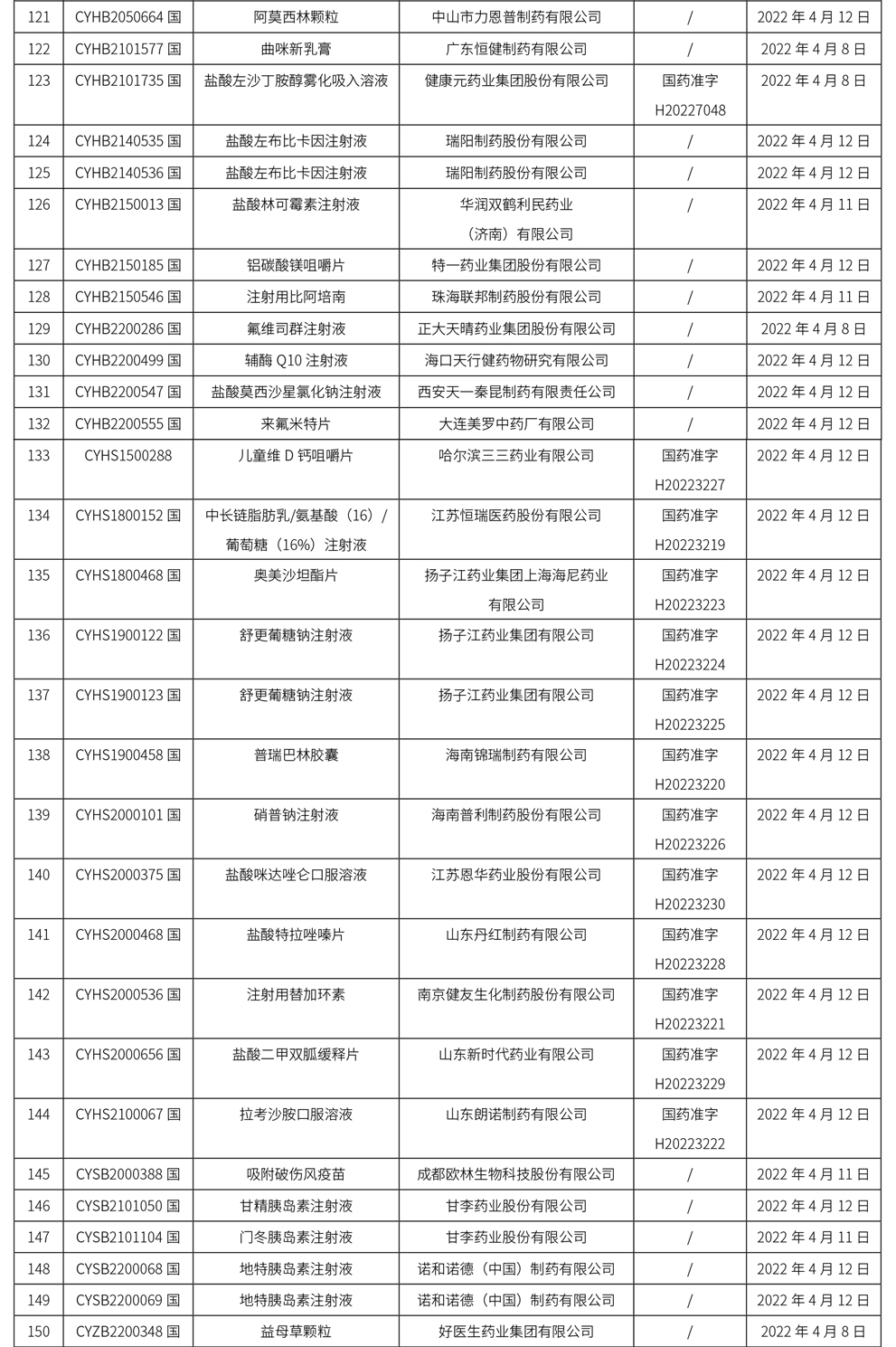
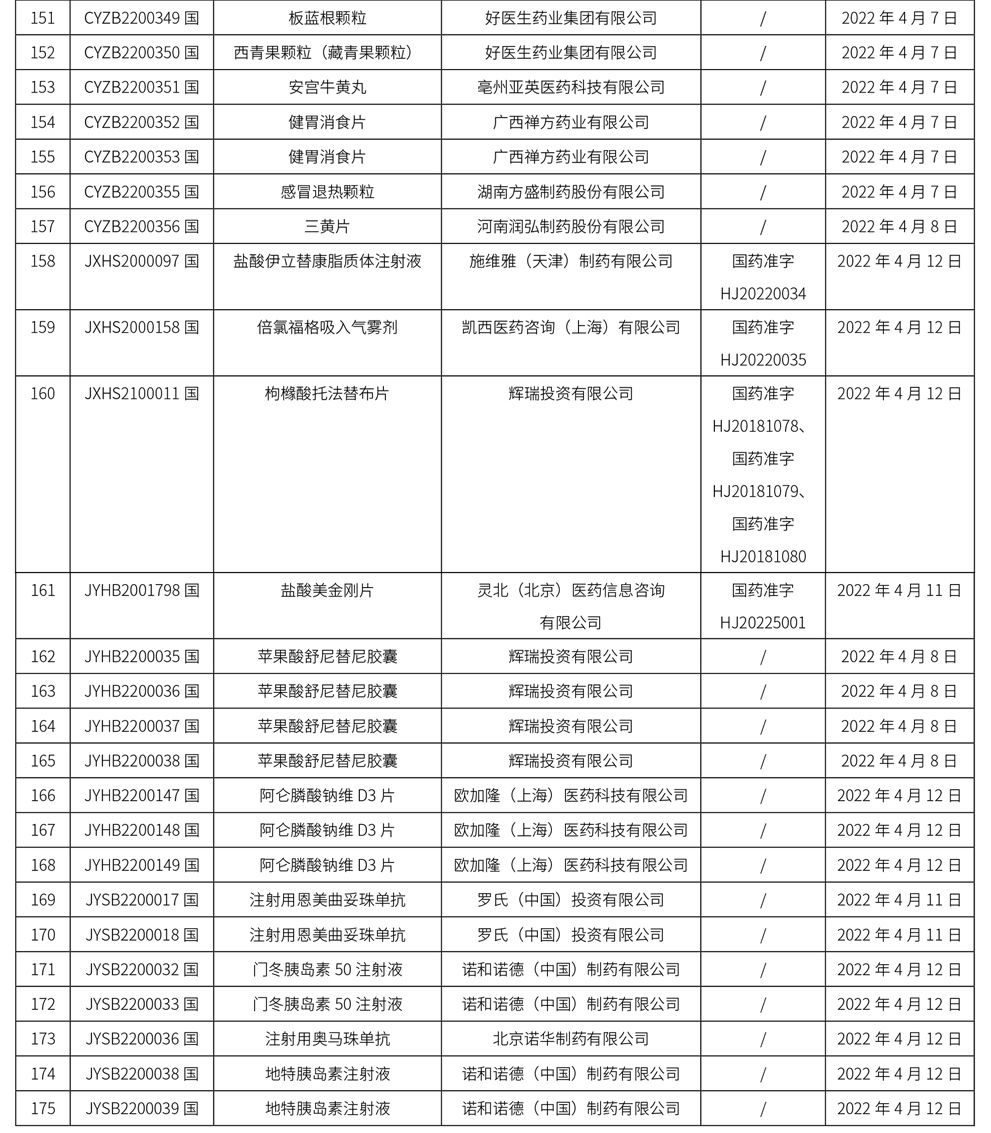
药典委
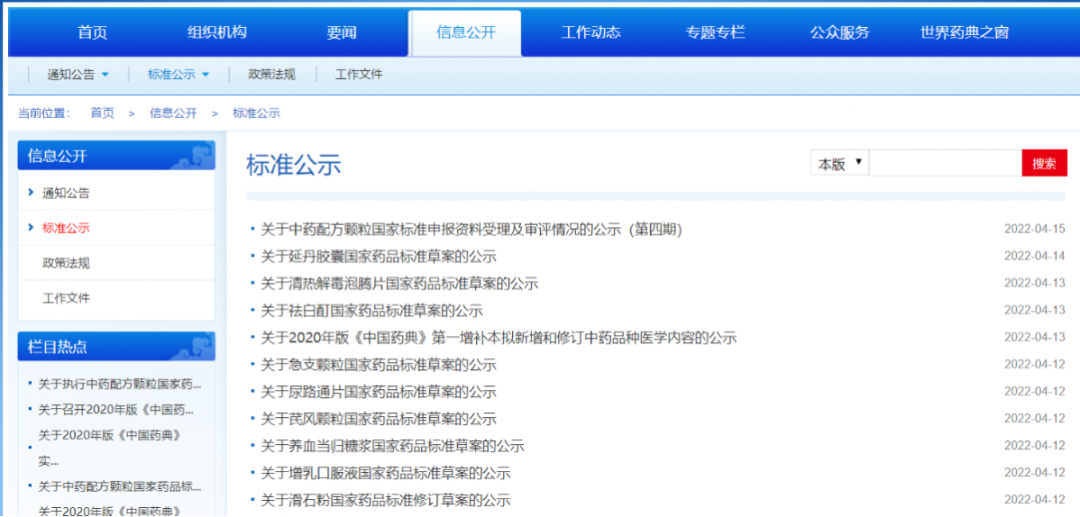
本周共发布18个品种国家标准草案/国家标准修订草案,及关于中药配方颗粒国家标准申报资料受理及审评情况、2020版《中国药典》第一增补本拟新增和修订中药品种医学内容的公示。
长按识别图中二维码
查看详细信息

-END-



转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450